[ad_1]
Bienvenido naturaleza Lectores, ¿les gustaría recibir este informe en su bandeja de entrada de forma gratuita todos los días? Regístrate aquí.
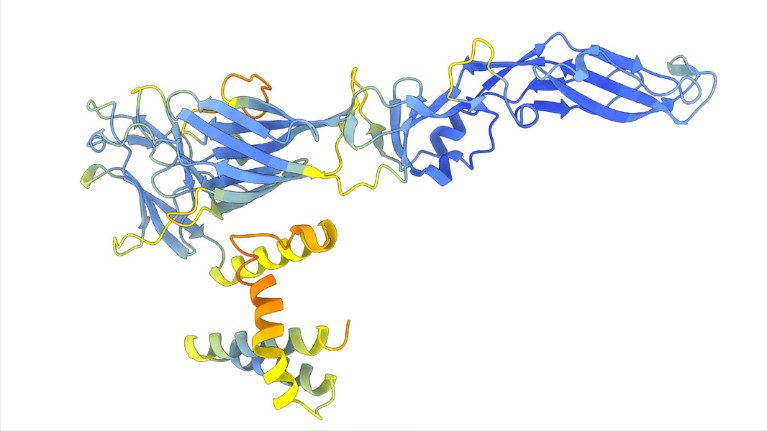
Copyright: Spyros Lytras y Joe Groff
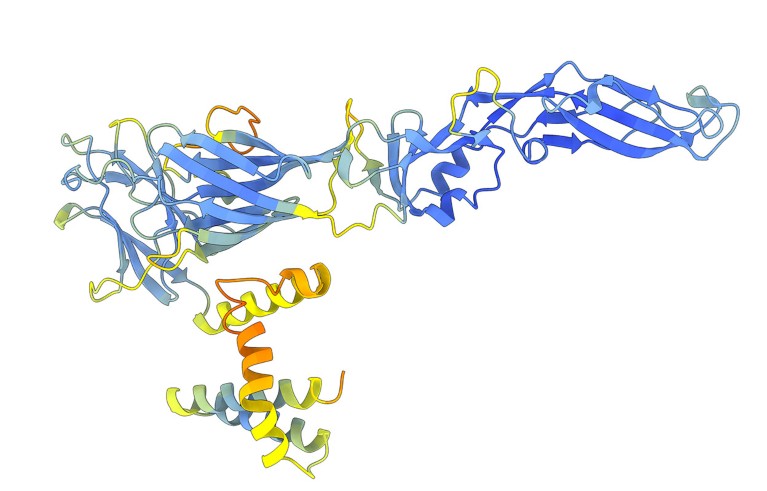
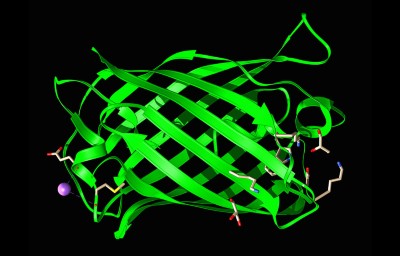
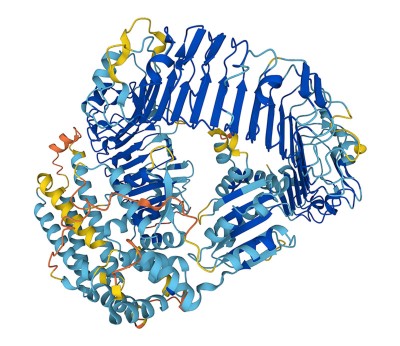
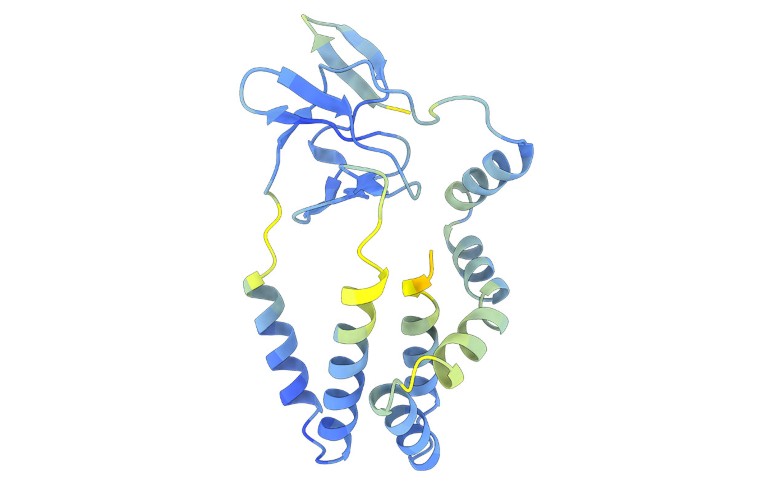
Las estructuras de las proteínas predichas por modelos de inteligencia artificial han revelado algunas fluctuaciones en la evolución de los flavivirus, el grupo que incluye el virus de la hepatitis C, el dengue y el virus del Zika. Los investigadores utilizaron DeepMind Pliegue alfa 2 Y el programa ESMFold de Meta para generar más de 33.000 estructuras predichas Los investigadores han podido detectar proteínas de 458 especies de flavivirus. Ya han descubierto algunas sorpresas. Por ejemplo, el virus de la hepatitis C infecta las células mediante un sistema de entrada similar al que se encuentra en los virus de la pestis, un grupo que incluye patógenos animales como la peste porcina. Otra gran sorpresa fue el descubrimiento de que algunos flavivirus contienen una enzima que parece haber sido robada de una bacteria.
Naturaleza | 5 minutos para leer
referencia: naturaleza papel
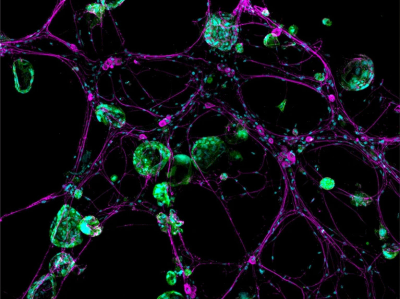
Altas temperaturas y fuertes lluvias Convertir a Europa en un caldo de cultivo para enfermedades transmitidas por mosquitosLos investigadores han advertido que este año ha habido 715 casos de transmisión local del virus del Nilo Occidental en 15 países europeos. El cambio climático está creando condiciones cómodas para el virus del Nilo Occidental. reinetas culex y Aedes albopictus Esto ha llevado a que los mosquitos se reproduzcan en lugares donde antes no podrían haber prosperado, ampliando su alcance y el período de transmisión de las enfermedades que transmiten. “Nos enfrentamos al problema de que nuevos lugares pueden convertirse en focos de transmisión de enfermedades que antes no estaban preparados para ello”, afirma la epidemióloga genética Houria Tejali.
Naturaleza | 5 minutos para leer
referencia: Informe del Centro Europeo para la Prevención y el Control de Enfermedades
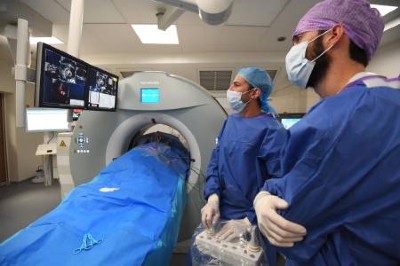
Los investigadores realizaron 26 exploraciones por resonancia magnética del cerebro de una mujer durante su primer embarazo para trazar un esquema sin precedentes de cómo estaba cambiando su cerebro. A la mujer de 38 años, que concibió mediante FIV, se le realizaron pruebas y muestras de sangre desde antes del embarazo hasta dos años después del nacimiento de su hijo. Mostrar datos Disminución generalizada de la materia gris y un aumento temporal de la materia blanca hacia el final del segundo trimestre.“El cerebro materno sufre este cambio regulado durante el embarazo y finalmente podemos monitorear el proceso en tiempo real”, dice la neurocientífica y coautora del estudio Emily Jacobs.
El guardián | 4 minutos para leer
Leer más: ¿Cómo afecta el embarazo al cerebro? (Naturaleza | 9 minutos para leer, naturaleza (muro de pago)
referencia: Neurociencia Natural papel
Seguir trabajando Se ha iniciado oficialmente el trabajo para desarrollar una supercomputadora que pueda superar en rendimiento a la computadora más rápida del mundo actual en aproximadamente 1.000 veces.Se espera que el dispositivo Fugaku Next le cueste al gobierno japonés unos 775 millones de dólares y esté previsto que esté operativo en 2030. La supercomputadora más rápida del mundo opera actualmente en el rango de quintillones (10 millones de millones de números).18) cálculos por segundo, o exaflops. Se espera que Fugaku Next funcione en el rango de zettaflops, 1.000 veces esa velocidad.
Mecánica Popular | lectura de 3 minutos
Características y opinión
Hay un número cada vez mayor de esfuerzos industriales y académicos que se están realizando Construya modelos de IA capaces de extrapolar principios biológicos básicos basados en proteínas, ARN, ADN o incluso datos de imágenes celulares.Estos principios se utilizan luego para guiar diversas tareas analíticas o de diseño. Muchos de estos modelos se describen como “modelos básicos”, un término que describe ampliamente sistemas que funcionan bien en una variedad de problemas diferentes a través de un proceso de “entrenamiento previo” en conjuntos de datos masivos y sin etiquetar. Esto contrasta con la mayoría de los algoritmos de aprendizaje profundo y automático en biología, que tienden a centrarse en tareas muy específicas.
Biotecnología Natural | Leer durante 10 minutos
La naturaleza universal de la ciencia, con su lenguaje y sus métodos supuestamente neutrales, proporciona un terreno común para la comunicación entre las personas y, por lo tanto, puede ayudar a construir relaciones pacíficas entre las naciones. Al menos, ese es un argumento que se esgrime a menudo, y los historiadores de la ciencia Roberto Lalli y Jaume Navarro lo analizan en un artículo para naturaleza. Están explorando muchos Las formas en que los físicos, tanto individual como colectivamente, han abordado las tensiones geopolíticas a lo largo del siglo XX¿Y qué pueden aprender de esto los académicos en general cuando analizan las respuestas, por ejemplo, a la guerra en curso en Ucrania?
Naturaleza | 10 minutos para leer
En su nuevo libro, Tierra quemada: una breve historiaSunil Amrith narra Las batallas de los pobres y débiles contra quienes buscan lucrar con los recursos naturales del planeta A lo largo de la historia. Como testimonio de perseverancia, Amrith relata las rebeliones ambientalistas de los últimos seiscientos años “brillantemente, en su exploración épica de la innovación y la destrucción humana”, como escribe Josie Glaucius, mientras nos lleva a los movimientos que aún hoy luchan por el futuro de la Tierra. .
Hoy intento descifrar Hounds and Jackals, uno de los juegos de mesa más antiguos que se conocen. Se pensaba que su origen se remontaba al antiguo Egipto, pero los arqueólogos acaban de descubrirlo. Encontré un cuadro en Azerbaiyán. – sugiriendo que tiene raíces más antiguas en Asia.
Cuéntanos a qué estás jugando, así como cualquier otro comentario en este boletín, en informació[email protected].
gracias por leer
Jacob Smith, editor asociado, Nature Review
Con contribuciones de Flora Graham y Sarah Tomlin
¿Quieres más? Suscríbase a nuestros otros boletines gratuitos de Nature Briefing:
• Información sobre la naturaleza: empleos – Información, consejos y periodismo galardonado para ayudarle a mejorar su vida laboral
• Nature Digest: Microbiología – Los organismos más abundantes en nuestro planeta -los microorganismos- y el papel que desempeñan en la salud, el medio ambiente y los sistemas alimentarios.
• Resumen de la naturaleza: el antropoceno – Cambio climático, biodiversidad, sostenibilidad y geoingeniería
• Nature Brief: Inteligencia artificial y robótica – Escrito por 100% humanos, por supuesto.
• Resumen de la naturaleza: Cáncer – Un boletín semanal escrito pensando en los investigadores del cáncer.
• Resumen de la naturaleza: investigación traslacional – Cubre biotecnología, descubrimiento de fármacos y farmacología.
[ad_2]
Source Article Link